了解分类、监管途径和医疗器械豁免
医疗设备的世界是多方面的,了解它们的分类是基本的. 在这篇博文中,我们将深入研究第2类医疗设备的领域. 我们不仅将探讨它们是什么,而且还将探讨为什么它们是医疗设备开发行业的关键组成部分.
2类分类过程和监管考虑
二班 医疗设备特别是以其中等风险水平而闻名. 将器械分类为第2类需要考虑几个关键因素:
- 基于潜在危害的风险评估:2类器械是指对患者存在中度风险的器械. 该风险评估考虑了器械的预期用途和潜在危害等因素.
- 特定法规控制的应用:确保第2类器械的安全性和有效性, 采用了具体的监管控制和绩效标准. 这些控制可能涉及设计、制造和质量管理.
- 对现有类似装置(谓词装置)的依赖:经常, 第2类设备与现有设备进行比较,称为谓词设备. 这种比较有助于简化监管审批过程,因为它将新设备与那些已被证明有记录的设备进行了比较.
- 复杂设备的专家分类小组:在某些情况下, 特别是对于复杂的设备, 专家小组被召集来对设备进行适当的评估和分类. 这样做是为了确保设备的分类与其潜在风险和收益保持一致.
- 没有合适的谓词的新设备的重新设计过程:对于没有合适的谓词设备进行比较的新设备, FDA提供De Novo过程. 该途径允许制造商为其创新产品建立分类和监管要求.
然而,二类医疗器械的成功发展并不止步于监管分类. 它还包括像设计思维这样的整体方法. 了解更多关于设计思维在医疗设备开发中的作用 在这里.
2类医疗器械的例子有哪些?
第2类医疗器械包括范围广泛的医疗保健技术, 了解这些例子可以为了解它们的多样性提供有价值的见解:
诊断设备:
- 心电图机:这些设备监测并记录心脏的电活动, 帮助诊断各种心脏疾病.
- 血糖监测器:对控制糖尿病至关重要, 这些设备允许患者定期监测他们的血糖水平.
手术器械:
- 外科剪刀:外科医生在手术中切割组织时使用的精密仪器.
- 输液泵:输送液体的装置, 比如药物和营养物质, 给病人静脉注射.
患者监护设备:
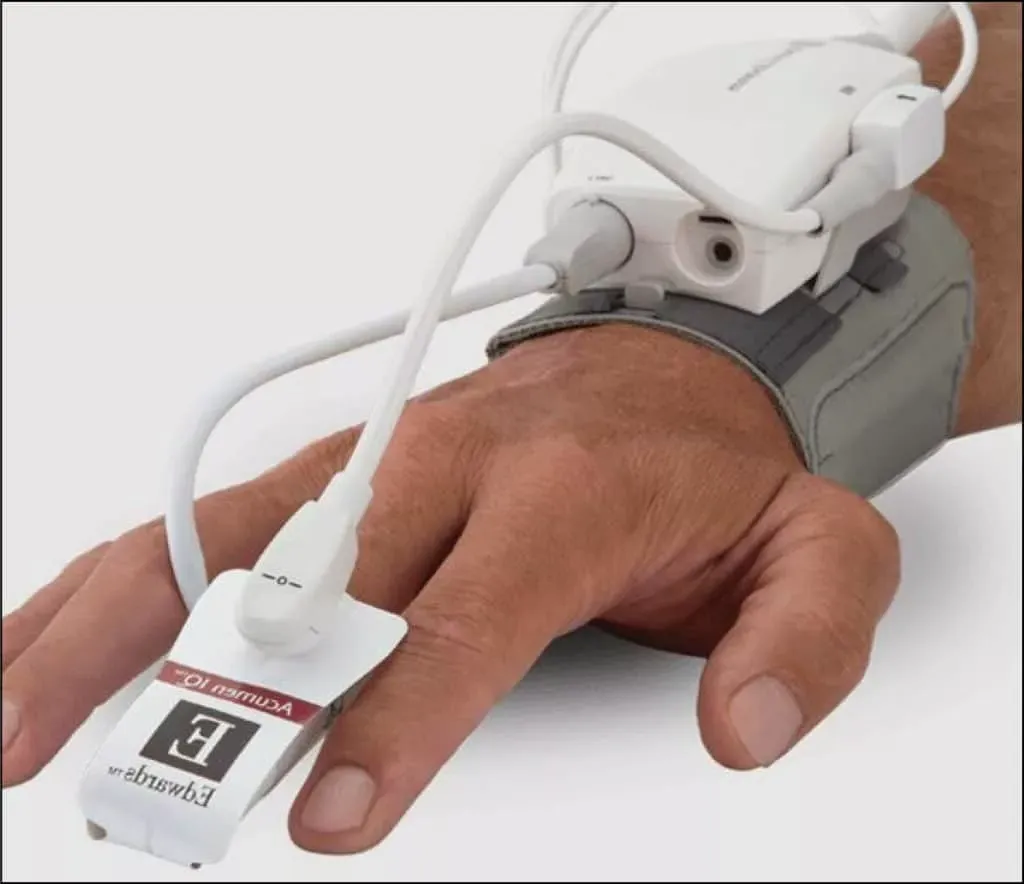
- 脉搏血氧仪:这些设备测量血液中的氧饱和度, 对监测病人的呼吸系统健康至关重要.
- 连续血糖监测仪:糖尿病管理的先进工具, 提供实时血糖水平数据.
骨科设备:
- 膝关节支架:用于支撑和稳定膝关节, 帮助膝盖损伤的恢复和康复.
- 脊柱植入物:在脊柱手术中用于治疗各种疾病和损伤的创新设备.
基于软件的医疗设备:
- 医学成像软件:用于处理和解释医学图像的高级软件, 包括x射线, 核磁共振成像, 和CT扫描.
- 远程医疗平台:近年来, 远程医疗软件已经崭露头角, 允许远程医疗保健咨询和监控.
2类器械的上市前申报有哪些不同?
如果你正在开发二类医疗设备,你需要通过FDA的监管途径. 有两种主要的上市前提交选择:
上市前通知书510(k):
510(k)通路通常用于2类器件. 它涉及证明你的器械实质上等同于合法销售的谓词器械. 需要考虑的要点:
- 文件:准备一个全面的提交包, 包括设备描述, 预期用途, 以及性能数据.
- 实质等同:强调你的器械在材料方面与谓词器械相似, 设计, 和预期用途.
- 性能测试**:进行性能测试以验证您的设备的安全性和有效性.
新创:
De Novo工艺适用于没有适当的谓词装置进行比较的新装置. 这需要做些什么:
- 提交:提交De Novo请求, 包括设备设计的详细信息, 预期用途, 性能特点.
- 审查和分类:FDA审查你的提交并将你的器械分类为1类, 2, 或者根据风险和收益来计算.
- 建立控制:一旦分类, FDA为你们的器械建立了特定的监管控制,以确保其安全性和有效性.
了解这些上市前提交选项对于成功将2类医疗器械推向市场至关重要.
2类器械有哪些豁免?
器械豁免可以简化某些2类医疗器械的监管过程. 以下是对设备豁免的深入分析:
具体的监管豁免:
豁免资格:一些2类器械可能有资格获得特定的法规豁免. 这些豁免通常在设备风险最小的情况下授予, 为了确保安全性和有效性,额外的控制是不必要的.
FDA决定:FDA根据其预期用途确定哪些2类器械有资格获得豁免, 风险, 历史安全数据.
豁免的例子:
I类豁免:如果某些2类器械构成最小风险并符合特定标准,则可以授予I类豁免. 这些豁免简化了监管程序, 减少审批所需的时间和资源.
豁免的好处:利用器械豁免可以加快开发, 批准, 以及二类设备的市场准入. 然而,理解这些豁免的含义和限制是至关重要的.
通过策略性地利用设备豁免, 制造商可以更有效地驾驭监管环境,同时确保他们的2类设备符合必要的安全标准.
Summary
总之, 第2类医疗器械是医疗保健行业的关键部分, 为患者护理和治疗提供多样化的解决方案. 了解它们的分类, 监管途径, 潜在的豁免对于寻求成功开发和销售这些设备的制造商至关重要. 通过这样做, 您可以为医疗技术的进步做出贡献,同时确保合规性和患者安全.